一、实验目的
1.掌握电导分析法的基本原理;
2.学会用电导法测定水纯度的实验方法;
3.掌握电导池常数的测量技术。
二、方法原理
水溶液中的离子,在电场作用下具有导电能力。导电能力称为电导G,其单位是西门子(S=Ω-1)。电导G与电阻R的关系是:
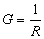
而导体的电阻与其长度l和截面积A的关系可用下式表示:
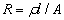
式中ρ称为电阻率,单位为Ω∙cm。电阻率的倒数1/ρ称为电导率κ,由此,电导与电导率关系可表示为:

式中θ称为电导池常数,是电极间距离l与其面积A之比。一支电极的电导池常数为确定值。
水质纯度的一项重要指标是其电导率的大小。电导率愈小,即水中离子总量愈小,水质纯度就高;反之,电导率愈大,离子总量愈大,水质纯度就低。普通蒸馏水的电导率约为3~5×10-6S∙cm-1,而去离子水可达1×10-7S∙cm-1。
三、仪器设备与试剂材料
1.电导仪,电导电极(光亮电极和铂黑电极)。
2.水样:去离子水、蒸馏水、自来水。
3.KCl标准溶液:准确称取已烘干的KCl(基准试剂)0.7455g置于小烧杯中用少量高纯水溶解,完全转入100mL容量瓶中,用高纯水配成0.1000mol∙L-1
KCl标准溶液。
四、实验步骤
1.电导池常数的测定
(1)将电导仪接上电源,开机预热。装上电导电极,用蒸馏水冲洗几次,并用滤纸吸去水珠。
(2)将洗净的电极再用KCl标准溶液清洗,并用滤纸沾去水珠。随后浸入欲测的KCl标准溶液中,启动测量开关进行测量。由测量结果确定电导池常数。
2.水样电导率的测定
取去离子水、蒸馏水、自来水分别置于3个50mL烧杯中,用蒸馏水、欲测水样依次清洗电极,逐一进行测量。
五、数据处理
1.计算出所使用的电导电极的池常数。
2.计算出测定水样的电导率和电阻率。
六、问题讨论
1.测量电导,为什么要用交流电源?能不能用直流电源?
2.电导法测量高纯度水时,随试液在空气中的放置时间增长,电导而增大,可能影响的因素是什么?
|