一、实验目的
1.掌握HClO4-HOAc非水滴定有机碱的原理和方法;
2.了解自动滴定管的使用要点;
3.巩固电位滴定曲线的绘制和终点的确定方法。
二、方法原理
药物中的碱性物质,比如胺类、生物碱、含氮杂环化合物、有机碱及氨基酸等,可在冰醋酸(或惰性溶剂)中,用HClO4进行滴定。检测终点的方法有指示剂法、电位法等。常用的指示剂是甲基紫、结晶紫,而电位法一般以玻璃电极为指示电极、饱和甘汞电极为参比电极,通过绘制滴定曲线来确定终点。
在非水介质中滴定碱时,常用的溶剂为冰醋酸。常用高氯酸的冰醋酸溶液为滴定剂,配制滴定剂时带来的水分一般通过加入一定量的醋酸酐除去。HClO4-HOAc滴定剂一般用邻苯二甲酸氢钾作为基准物质进行标定:
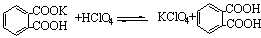
三、仪器设备与试剂材料
1.pHS-2型酸度计或数字离子计,甘汞电极,玻璃电极,磁力搅拌器。
2.10mL自动滴定管(最小分度0.05mL)及500mL贮液瓶。
3.冰醋酸(A.R.),醋酸酐(A.R.),高氯酸(70%~72%),邻苯二甲酸氢钾(基准试剂),2g∙L-1结晶紫冰醋酸溶液。
4.待测有机碱样品。
四、实验步骤
以下所用的量具、容器应充分干燥(110~120℃烘2小时)。
1.HClO4-HOAc溶液的配制和标定
取1000mL烧杯一只,加入冰醋酸约800mL,加入70%~72%高氯酸8.5mL混匀,缓缓滴加醋酸酐23mL,混匀,冷至室温。再用冰醋酸稀释成1000mL,转移至试剂瓶中,放置24小时使醋酸酐与溶液中的水充分反应。
将配制好的HClO4-HOAc溶剂倒入自动滴定管的储液瓶中并充至滴定管的零刻度线。
准确称取已在110℃干燥2小时的邻苯二甲酸氢钾约0.16g置于125mL锥形瓶中,加冰醋酸20mL,使其完全溶解,加结晶紫指示剂1滴,用待标定的HClO4-HOAc溶液滴定,溶液颜色由紫色变为蓝色即为终点。
计算HClO4-HOAc溶液的浓度(mol∙L-1):
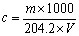
式中:m-邻苯二甲酸氢钾质量,单位为g;
V-滴定至终点HClO4-HOAc溶液消耗的体积,单位为mL。
另取20mL冰醋酸按上述操作作空白滴定,取得空白值以校正上述结果。
2.电位滴定
准确称取一定量的待测样品,置于100mL的烧杯中,加入醋酸酐-冰醋酸(5+1)的混合液25mL,微热使之溶解并冷至室温。放入搅拌磁子,将玻璃电极和饱和甘汞电极浸入溶液中,并与酸度计连接(酸度计使用mV档),将滴定管尖端插进溶液中,开动电磁搅拌器,测定并记录起始电动势E。以HClO4-HOAc溶液滴定并记录相应的E值,直至超过计量点数毫升为止。
同时,以25mL醋酸酐-冰醋酸(5+1)混合液,按上述操作作空白滴定。
五、数据处理
1.以加入的HClO4-HOAc溶液体积为横坐标,相应的E值为纵坐标,绘制滴定曲线,并由滴定曲线确定终点。
2.按下式计算试样中有机碱的质量分数:
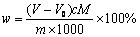
式中:w--有机碱质量分数;
m--试样质量,单位g;
c--HClO4-HOAc标准溶液浓度,单位为mol∙L-1;
M—有机碱的摩尔质量,单位为g∙mol-1;
V—至滴定终点HClO4-HOAc溶液消耗的体积,单位为mL;
V0—空白滴定中HClO4-HOAc溶液消耗的体积,单位为mL。
六、问题讨论
1.为什么在标定的测定中都要作空白试验?
2.整个滴定中水分的存在会有什么影响?