一、实验目的
1.熟悉极谱分析的基本原理;
2.掌握在极谱测量中消除干扰电流的方法。
二、方法原理
极谱法是在静止溶液中以滴汞电极(DME)为工作电极的伏安方法。在通常的极谱分析中,滴汞周期为3~5s,施加在滴汞电极上的线性变化电压很慢,约为0.2V∙min-1。记录连续滴落汞滴上的i~E曲线呈S形,称为极谱图。
滴汞电极的“电位窗口”相对参比电极在负值区,溶液中的溶解氧在此范围产生两个还原波,干扰大多数物质的测定,必须采取适当的方法以消除氧的干扰。在不同的介质中,需选用不同的除氧方法。本实验是在中性溶液中,可通纯N2除氧。
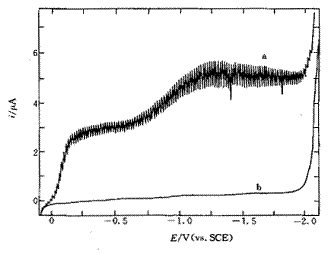
0.1mol∙L-1
KCl的极谱图
a.用空气饱和 b.氮气除氧后
极谱分析时,一些物质在滴汞电极上反应,电流随极化电压的增加而迅速增加到一极大值,然后下降到扩散电流的正常值。这种极谱曲线上出现的比扩散电流大得多的不正常“电流畸峰”,称为“极谱极大”。影响极谱极大的产生、形成、形状以及大小的因素很多。一般说来,溶液愈稀,极大现象也就愈明显。然而极大的大小与被测物的浓度没有简单关系,故应加以除去。在溶液中加入少量的表面活性物质,能抑制极大现象。常用的试剂有明胶、聚乙烯醇、TritonX-100等。
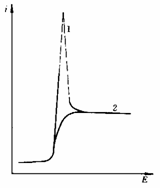
极谱极大
1-极大极谱波;2-消除极大极谱波
迁移电流是被测离子在外加电场的作用下,正离子向负极移动,负离子向正极移动,并分别在电极上被还原和氧化所产生的电流。迁移电流与被测离子没有定量关系,故必须除去。消除的方法是在极谱试液中加入大量的“惰性支持电解质”。常用的惰性支持电解质有KCl、KNO3、NH4Cl、HCl等。
三、仪器设备与试剂材料
1.笔录式极谱仪。
2.氯化钾溶液:0.1mol∙L-1,0.01mol∙L-1。
3.0.010mol∙L-1 PbCl2溶液。
4.0.5%明胶溶液。
四、实验步骤
1.溶解氧的极谱波和极大现象
取1.0mL 0.01mol∙L-1 KCl溶液,置极谱电解池中,再加入9.0mL蒸馏水,采用移液管挤入空气气泡,使试液中的溶解氧尽量达到饱和。然后提高储汞瓶,待汞滴流出后,用蒸馏水吹洗电极,并用滤纸吸干,插入电解池的试液中,调节汞柱高度,使滴汞周期为3~5s。在外加电压0~-2.0V间,记录极谱波。
2.极大现象的抑制
在上述测量溶液中,滴加2滴明胶(此时明胶的浓度约为0.005%),搅匀。在0~-2.0V电压之间记录极谱图。
3.氧波的消除
向步骤2的测定溶液中通纯氮气10min,然后再次记录极谱波。
4.迁移电流及其消除
(1)取0.01mol∙L-1
PbCl2 1.0mL于10mL小烧杯中,滴加0.5%明胶2滴,加蒸馏水9.0mL,通纯氮气5min,在-0.2~0.7V间记录极谱图。
(2)分别取0.01mol∙L-1
PbCl2 1.0mL置于两个10mL小烧杯中,其中一个烧杯中加入0.1mol∙L-1
KCl溶液9.0mL,别一个烧杯中加入0.01mol∙L-1
KCl溶液9.0mL。分别滴加0.5%明胶2滴,通N2气5min,在-0.2~0.7之间记录它们的极谱图。
实验完毕后,移去电解池,用蒸馏水吹洗电极几次,滤纸沾干后,降下储汞瓶。清理实验中滴落的废汞,储于安全地方。
五、数据处理
1.用文字注明每幅极谱图的实验条件。
2.列表记录Pb2+的极谱电流id与KCl浓度的关系。
六、问题讨论
1.比较氧波、极大及除氧后的极谱波,并写出氧在滴汞电极上的化学反应式。
2.简述极谱测定中的除氧方法。
3.如果阴离子在滴汞电极上还原时,由于迁移电流的存在,将会如何影响被测物质的测量结果?