|
一、实验目的
1.了解硫化氢系统分析法的离子分组,组试剂和分组分离条件。
2.总结、比较常见阳离子的有关性质。
3.将Cu2+、Sn4+、Cr3+、Ni2+、NH4+和Hg2+、Cu2+、Pb2+、Ni2+、Mg2+等离子进行分离检出,并掌握其分离检出条件。
4.自行拟定两组阳离子分离检出的实验方案。
二、实验原理
在水溶液中,离子的分离与检出是以各离子对试剂的不同反应为依据的。这种反应常伴有特殊的现象。例如,沉淀的产生、特征颜色和气体产生等,各种离子对试剂作用的相似性和差异性就构成了离子分离和检出方法的基础,即离子本身的性质是分离检出的基础。
任何分离、检出反应都是在一定条件下进行的,选择适当的条件(如溶液的酸度,反应物浓度、温度等)可以使反应向我们预计的方向进行,因此在设计水溶液中混合阳离子分离检出实验方案时,除了必须熟悉各种离子的性质外,还会运用离子平衡(酸碱、沉淀、氧化还原和配合平衡)的规律控制反应条件。这样既利于我们熟悉离子性质,又利于加深对各类离子平衡的理解。
对于组分较复杂试样的离子分离与检出,通常采用系统分析法,常用的经典系统分析法有两种,硫化氢系统分析法和两酸两碱系统分析法,由于硫化氢系统分析法应用较广泛,我们主要介绍硫化氢系统分析法。
在系统分析中,首先用几种组试剂将溶液中性质相似的离子分成若干组,然后在组内进行分离和检出。所谓“组试剂”是指能将几种离子同时沉淀出来而与其它离子分开的试剂。
硫化氢系统分析法是以硫化物溶解度的不同为基础,用4种组试剂把常见的阳离子分为5个组的系统分析法,常见阳离子的分组情况及所用组试剂列入表18-1:
硫化氢系统分析的过程是:在含有阳离子的酸性溶液中加入HCl;Ag+、Pb2+、Hg22+形成白色的氯化物沉淀,而与其他阳离子分离,这几种阳离子就构成了盐酸组。沉淀盐酸组时,HCl的浓度不能太大,否则会因形成配合物而沉淀不完全。在分离沉淀后的清液中调节至HCl的浓度为0.3mol·dm-3,通入H2S(或加硫代乙酰胺并加热),Pb2+、Bi3+、Cu2+、Cd2+、Hg2+、As(Ⅲ,V),Sb(Ⅲ,V),Sn4+等阳离子生成相应的硫化物沉淀,这些离子组成了硫化氢组,这些离子除Pb2+外,其氯化物都溶于H2O,Pb2+,虽然在盐酸组中析出一部分PbCl2沉淀,但由于沉淀不完全,溶液中还剩相当量的Pb2+,所以硫化氢组中也包括Pb2+。在分离沉淀后的清液中加入氨水至碱性(NH4C1存在下),通入H2S(或加入硫代乙酰胺并加热),Fe3+、Co2+、Ni2+、Mn2+、Zn2+形成硫化物沉淀,而Al3+、Cr3+形成氢氧化物沉淀,这些离子统称为硫化铵组。在沉淀这一组离子时,溶液的酸度不能太高,否则本组离子不可能沉淀完全,溶液酸度也不可能低,否则另一组的Mg2+可能部分生成Mg(OH)2沉淀,并且A1(OH)3呈两性也可能部分溶解,于是溶液中加入一定量的NH4Cl以控制溶液的pH值,防止形成Mg(OH)2沉淀和A1(OH)3的部分溶解。在分离沉淀后的清液中加入(NH4)2CO3,Sr2+,Ba2+和Ca2+形成碳酸盐并析出沉淀,称为碳酸铵组,剩下的Mg2+,K+,Na+,NH4+不被上述任何组试剂所沉淀。留在溶液中,叫易溶组,这一分析过程见图18-1。分成5个组后再利用组内离子性质的差异性,利用各种试剂和方法一一进行检出。
表18-1阳离子的硫化氢系统分组
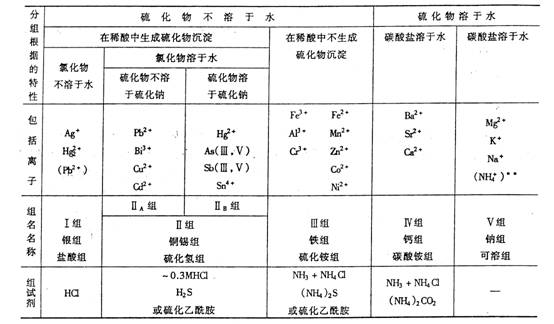
*Pb2+浓度大时部分沉淀。
**系统分析中需要加入铵盐,故NH4+需另行检出。
三、仪器和药品
离心机,恒温水浴
Cu2+,Sn4+,Cr3+,Ni2+,Ca2+,NH4+的混合液;Hg2+,Cu2+,Pb2+,Ni2+,Mg2+的混合液;2mol·dm-3 NaOH溶液,6mol·dm-3氨水。6mol·dm-3 HCl溶液,5%硫代乙酰胺溶液;Zn粉;0.2mol·dm-3 HgCl溶液;2mol·dm-3 HNO3;lmol·dm-3 NaAc溶液;0.25mol·dm-3 K4Fe(CN)6溶液;6mol·dm-3 NaOH溶液;6%H2O2;6mol·dm-3 HNO3;1%丁二酮肟溶液;lmol·dm-3 (NH4)2CO3溶液;2mol·dm-3 HAc溶液,1%乙二醛双缩(α-羟基苯胺)(简称GBHA)的乙醇液液;10%NaOH溶液;10% Na2CO3溶液;CHCl3;1.0mol·dm-3 H2SO4;饱和NH4Ac溶液;lmol·dm-3 K2CrO4溶液;lmol·dm-3 KI溶液;2% CuSO4溶液;Na2SO3(固体);2mol·dm-3 氨水;0.001%镁试剂I(对硝基苯偶氮间苯二酚);百里酚蓝指示剂;0.1%甲基紫指示剂;3mol·dm-3 NH4Cl。
以上溶液的配制可以参阅高等教育出版社出版的,由武汉大学主编的《分析化学实验》第二版,P134~147。
四、实验内容
1.Cu2+,Sn4+,Cr3+,Ni2+,Ca2+,NH4+混合液的定性分析
系统分析图如图18-2
操作步骤
(1)初步检验——NH4+的鉴定,首先将一小块pH试纸用蒸馏水润湿,贴在表面皿中心,另一表面皿中加2滴混合液,2滴2mol·dm-3 NaOH溶液,很快用贴有pH试纸的表面皿盖上,将此气室放在水浴上加热,如pH试纸变为碱色,示有NH4+存在。
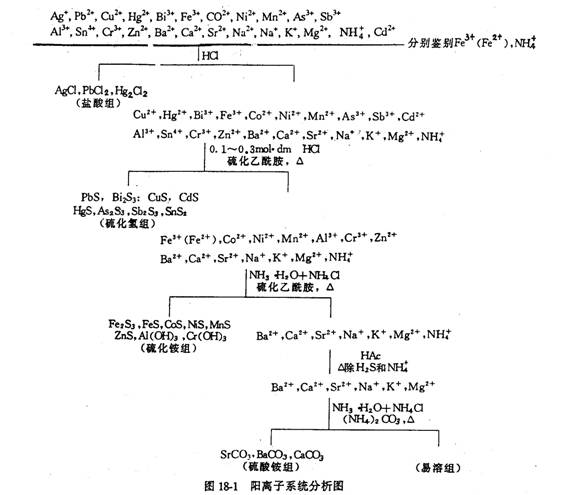
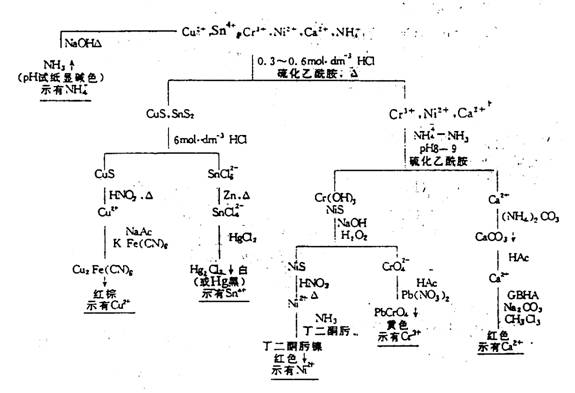
图18-2 Cu2+、Sn2+、Cr2+、Ca2+、 的系统分离、检出图 的系统分离、检出图
(2)各离子的分离与检出
a.Cu2+、Sn4+与Cr3+,Ni2+,Ca2+的分离以及Cu2+、Sn4+的检出,取20滴混合液于1支离心试管中,加入1滴0.1%甲基紫指示剂,用NH3和HCl调至溶液为绿色,加入10滴5%硫代乙酰胺,加热,则析出CuS和SnS2沉淀,离心分离(离心液按(b)处理)沉淀用含HCl的水洗二次,弃去洗涤液,沉淀上加4~5滴6mol·dm-3
HCl,充分搅拌,加热,使SnS2充分溶解,离心分离,离心液为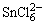 ,用少许Zn粉将其还原为 ,用少许Zn粉将其还原为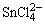 ,取此溶液2滴,加入1滴0.2mol·dm-3 HgCl2,生成白色沉淀,并逐渐变为黑色,证明有Sn4+存在。CuS沉淀用含HCI水洗涤,弃去洗涤液,加2滴2mol·dm-3 HNO3,加热溶解,并除去低价氮的氧化物,离心分离,弃去沉淀,溶液加1mol·dm-3
NaAc和0.25mol·dm-3 K4Fe(CN)6溶液各一滴,生成红棕色沉淀,证明有Cu2+存在。 ,取此溶液2滴,加入1滴0.2mol·dm-3 HgCl2,生成白色沉淀,并逐渐变为黑色,证明有Sn4+存在。CuS沉淀用含HCI水洗涤,弃去洗涤液,加2滴2mol·dm-3 HNO3,加热溶解,并除去低价氮的氧化物,离心分离,弃去沉淀,溶液加1mol·dm-3
NaAc和0.25mol·dm-3 K4Fe(CN)6溶液各一滴,生成红棕色沉淀,证明有Cu2+存在。
b.Cr3+,Ni2+与Ca2+的分离和Cr3+,Ni2+的鉴定,在(a)的离心液中,加入5滴3mol·dm-3溶液及百里酚蓝指示剂,再用15mol·dm-3
NH3水及0.5mol·dm-3 NH3水调至溶液显黄棕色(先用浓氨水,后用稀氨水调节),加10滴5%硫代乙酰胺,在水浴中加热,离心分离,离心液按(c)处理。沉淀用1% NH4NO3溶液洗涤。弃去溶液,沉淀加3滴6mol·dm-3
NaOH和3滴6% H2O2,加热,使Cr(OH)3溶解,此时生成黄色的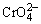 ,离心分离,离心液加HAc酸化,加1滴Pb2+溶液,生成黄色沉淀,示有Cr3+。 ,离心分离,离心液加HAc酸化,加1滴Pb2+溶液,生成黄色沉淀,示有Cr3+。
NiS沉淀用1% NH4NO3溶液洗涤,弃去溶液,沉淀上加2滴6mol·dm-3
HNO3,加热溶解,分离出生成的硫磺沉淀,清液中加入6mol·dm-3 NH3水,使之呈碱性,加1滴1%丁二酮肟,生成红色沉淀,证明有Ni2+存在。
(c)Ca2+的鉴定 在(b)的离心液中,加3滴1mol·dm-3
(NH4)2CO3,生成白色沉淀,离心分离,弃去离心液,沉淀用水洗一次,加2滴2mol·dm-3
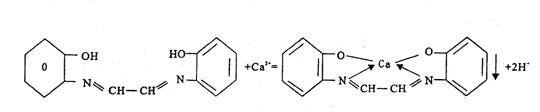
HAc溶解,取此溶液1滴,加4滴1% GBHA的乙醇溶液,1滴10% NaOH溶液,1滴10% Na2CO3溶液和3~4滴CHCl3,再加数滴水,摇动试管,CHCl3层显红色示有Ca2+存在。
2.Hg2+、Cu2+、Pb2+、Ni2+、Mg2+混合液的定性分析
系统分析示意图见图18-3
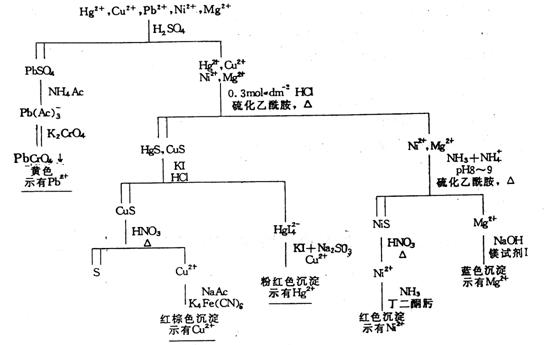
图18-3 Hg2+、Cu2+、Pb2+、Ni2+、Mg2+的分离,检出图
操作步骤
(1)Pb2+的分离和鉴定 取20滴混合试液,加数滴1mol·dm-3
H2SO4 使PbSO4沉淀完全,离心分离。离心液按(2)处理;沉淀用H2SO4洗一次,洗液并入离心液。沉淀用饱和NH4Ac溶解,加1~3滴1mol·dm-3
K2CrO4,生成黄色沉淀,示有Pb2+。
(2)Hg2+,Cu2+与Ni2+、Mg2+的分离和Hg2+、Cu2+的鉴定 取(1)的离心液,加1滴甲基紫指示剂,用NH3和HCl调节至溶液呈绿色,加数滴硫代乙酰胺,充分搅拌,在水浴中加热,离心沉降,用热水洗涤1-2次,离心液按(3)处理。
在上述沉淀上加2滴6mol·dm-3
HCl和6滴1mol·dm-3
KI充分搅动,使HgS溶解,离心分离,对沉淀重复处理两次,离心液合并,加入2滴2% CuSO4溶液及少许固体Na2SO3,生成桔红Cu2HgI4沉淀,示Hg2+存在。
在CuS沉淀上加2滴6mol·dm-3 HNO3,加热,将生成硫磺沉淀离心分离,在清液中加数滴1mol·dm-3
NaAc和1滴0.25mol·dm-3
K4Fe(CN)6,生成棕红色沉淀,示有Cu2+。
(3)Ni2+与Mg2+的分离和检出,在(2)的离心液中,加入数滴3mol·dm-3 NH4Cl及1滴百里酚蓝指示剂,再用NH3水调节至溶液呈绿色,加数滴硫代乙酰胺溶液,在水浴上加热,生成黑色NiS沉淀,离心分离,沉淀用含NH4NO3的热水洗涤后,加4~5滴2mol·dm-3
HNO3加热,NiS溶解后将生成的硫磺离心分离,溶液中加数滴2mol·dm-3
NH3水,呈微碱性,加2滴1%丁二酮肟,生成鲜红色沉淀,示有Ni2+。
分出NiS沉淀后的离心溶液中,加入6mol·dm-3 NaOH使溶液呈碱性,加1~2滴镁试剂I,生成蓝色沉淀,示有Mg2+。
五、预习要求
1.查阅有关的参考书,了解常见阳离子的化学性质、与组试剂反应后的产物性状以及相应反应方程式。
2.预习有关离心机,恒温水浴及固液分离的操作。
六、思考题
1.根据本实验的内容,总结常见离子的检出方法,写出反应条件、现象及反应方程式。
2.拟定下列两组阳离子的分离检出的实验方案:
(1) Cu2+ Ag+ Hg2+ Ba2+
(2)Na+ Ni2+ Pb2+ Cr2+ Ca2+
3.请选用一种试剂区别下列5种溶液
KCl,Cd(NO3)2,AgNO3,ZnSO4,CrCl3
4.各用一种试剂分离下列各组离子
(1)Zn2+和Al3+
(2)Cu2+和Hg2+
(3)Zn2+和Cd2+
七、附注(某些有机试剂的结构简式和有关阳离子的检出反应方程式)
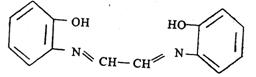
1.GBHA(乙二醛双缩(a-羟基苯胺))
2.丁二酮肟
CH3-C=NOH

CH3-C=NOH
3.硫代乙酰胺
S
CH3-C
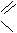
NH2
其水解反应式为
酸性溶液中: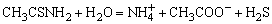
碱性溶液中: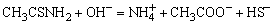
4.Cu2+的检出反应方程式:
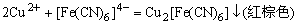
5.Hg2+的检出反应方程式:
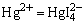
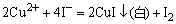
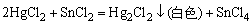
6.Pb2+检出反应方程式:
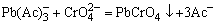
7.Sn4+的检出反应方程式:
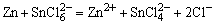
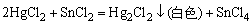
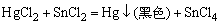
8.Cr3+的检出反应
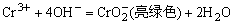
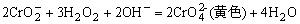
9.Ni2+的检出反应:
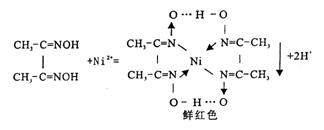
10.Ca2+的检出反应:
八、参考文献
1.普通化学实验(修定本),北京大学化学系普通化学教研室,北京大学出版社,北京,1991年,P252-275。
2.分析分学实验(第2版),武汉大学,高教育出版社,北京,1985年,P43-71。
3.无机离子快速检出法,韩葆玄,人民教育出版社,北京,1979年
|